
Clavaseptin 750 mg
1. Naam van het diergeneesmiddel
Clavaseptin 750 mg, tabletten voor honden
2. Samenstelling
Per tablet:
Werkzame bestanddelen:
Amoxicilline…………………………………………………600 mg
(Overeenkomend met amoxicillinetrihydraat)…………688,69 mg
Clavulaanzuur………………………………………………150 mg
(Overeenkomend met kaliumclavulanaat)……………..178,69 mg
Hulpstoffen:
IJzeroxide, bruin (E172)…………………. 1,43 mg
Langwerpige, gebroken wit tot bruinachtig gespikkelde tabletten met breuklijnen van ongeveer 24 mm. De tablet kan in vier gelijke delen worden verdeeld.
3. Doeldiersoorten
Hond.
4. Indicaties voor gebruik
Behandeling van infecties veroorzaakt door bacteriën gevoelig voor amoxicilline in combinatie met clavulaanzuur (inclusief beta-lactamaseproducerende stammen), in het bijzonder:
- Huidinfecties (inclusief diepe en oppervlakkige pyodermie, wonden, abcessen) veroorzaakt door Staphylococcus spp., Streptococcus spp. en Pasteurella spp.
- Luchtweginfecties (sinusitis, rhinotracheïtis, bronchopneumonie) veroorzaakt door Staphylococcus spp. en E. coli.
- Infecties van de mondholte (slijmvliezen) veroorzaakt door Streptococcus spp., en Pasteurella spp.
- Urineweginfecties (nefritis, cystitis) veroorzaakt door E. coli, Klebsiella spp. en Proteus mirabilis.
- Spijsverteringskanaalinfecties, vooral gastro-enteritis veroorzaakt door E. coli.
5. Contra-indicaties
Niet gebruiken bij overgevoeligheid voor penicillinen of andere stoffen uit de β-lactamgroep, of voor één van de hulpstoffen.
Niet toedienen aan gerbils, cavia’s, hamsters, konijnen en chinchilla’s of andere kleine planteneters.
Niet gebruiken bij dieren met ernstige nierfunctiestoornissen die gepaard gaan met anurie of oligurie.
Niet toedienen aan paarden en herkauwende dieren.
6. Speciale waarschuwingen
Speciale waarschuwingen:
Er is kruisresistentie aangetoond tussen amoxicilline/clavulaanzuur en β-lactamantibiotica. Gebruik van het diergeneesmiddel moet zorgvuldig worden overwogen wanneer gevoeligheidstests resistentie tegen β-lactamantibiotica hebben aangetoond, omdat de werkzaamheid dan verminderd kan zijn.
Meticillineresistente S. aureus (MRSA) en meticillineresistente S. pseudintermedius (MRSP) zijn geïsoleerd bij katten en honden met een resistentiepercentage dat varieert tussen EU-landen.
Niet gebruiken bij bekende resistentie tegen de combinatie van amoxicilline en clavulaanzuur. Niet gebruiken bij vermoedelijke of bevestigde MRSA/MRSP-infecties, aangezien isolaten als resistent moeten worden beschouwd tegen alle β-lactam, inclusief de combinatie amoxicilline/clavulaanzuur.
Hoge resistenties (tot 100%) zijn gemeld in E. coli-isolaten van huidinfecties en infecties van de weke delen bij honden.
Speciale voorzorgsmaatregelen voor veilig gebruik bij de doeldiersoort(en):
Bij dieren met een verminderde lever- en nierfunctie moet het gebruik van het diergeneesmiddel worden onderworpen aan een baten-risicobeoordeling door de dierenarts en moet de dosering zorgvuldig worden geëvalueerd.
Het gebruik van het geneesmiddel voor diergeneeskundig gebruik moet gebaseerd zijn op de identificatie van en gevoeligheidstests op de doelpathogeen of doelpathogenen.
Als dit niet mogelijk is, moet de therapie gebaseerd zijn op epidemiologische informatie en kennis van de gevoeligheid van de doelpathogenen op lokaal/regionaal niveau.
Het gebruik van het diergeneesmiddel moet in overeenstemming zijn met het officiële, nationale en lokale beleid ten aanzien van antimicrobiële middelen.
Aminopenicillinen in combinatie met beta-lactamaseremmers vallen in AMEG-categorie “C”. Een antibioticum met een lager risico op antimicrobiële resistentieselectie (lagere AMEG-categorie) dient gebruikt te worden voor eerstelijnsbehandeling waar gevoeligheidstestens de waarschijnlijke werkzaamheid van deze aanpak suggereren.
Een smalspectrumantibioticumbehandeling met een lager risico op antimicrobiële resistentieselectie dient gebruikt te worden voor eerstelijnsbehandeling waar gevoeligheidstestens de waarschijnlijke werkzaamheid van deze aanpak suggereren.
De tabletten bevatten smaakstoffen. Bewaar de tabletten buiten het bereik van de dieren om accidentele ingestie te voorkomen.
Er moet rekening worden gehouden met de mogelijkheid van allergische kruisreactiviteit met andere penicillines.
Speciale voorzorgsmaatregelen te nemen door de persoon die het diergeneesmiddel aan de dieren toedient:
Penicillinen en cefalosporinen kunnen overgevoeligheid (allergie) veroorzaken na injectie, inademen, ingestie of na contact met de huid. Overgevoeligheid voor penicillinen kan leiden tot kruisreacties met cefalosporinen, en vice versa. Allergische reacties veroorzaakt door deze stoffen kunnen in sommige gevallen ernstig zijn.
Werk niet met dit diergeneesmiddel als u overgevoelig bent of indien u geadviseerd bent om niet met dergelijke producten te werken.
Ga zeer voorzichtig om met dit diergeneesmiddel om blootstelling te voorkomen en neem alle aanbevolen voorzorgsmaatregelen in acht.
Als u na blootstelling symptomen zoals huiduitslag ontwikkelt, dient u een arts te raadplegen en deze waarschuwing te laten zien.
Zwelling van het gezicht, de lippen of de ogen, of ademhalingsmoeilijkheden zijn ernstiger symptomen die onmiddellijke medische verzorging vereisen.
Was de handen na het hanteren van de tabletten.
Accidentele ingestie van het diergeneesmiddel door een kind kan schadelijk zijn. Om accidentele ingestie te voorkomen, in het bijzonder door een kind, moeten ongebruikte deeltabletten worden teruggeplaatst in de open blisterruimte en weer in het doosje worden gedaan.
In geval van accidentele ingestie, dient onmiddellijk een arts te worden geraadpleegd en de bijsluiter of het etiket te worden getoond.
Dracht en lactatie:
De veiligheid van het diergeneesmiddel is niet bewezen tijdens dracht en lactatie. Uit laboratoriumonderzoek bij ratten zijn geen gegevens naar voren gekomen die wijzen op schadelijke effecten voor de foetus of het moederdier.
Uitsluitend gebruiken overeenkomstig de baten-risicobeoordeling door de behandelende dierenarts.
Interactie met andere geneesmiddelen en andere vormen van interactie:
De bactericide werking van amoxicilline kan worden verminderd door gelijktijdig gebruik van bacteriostatische stoffen zoals macroliden, tetracyclinen, sulfonamiden en chlooramfenicol.
Penicillines kunnen het effect van aminoglycosiden versterken.
Overdosering:
Bij driemaal de aanbevolen dosis gedurende 28 dagen werd diarree waargenomen bij honden. Bij overdosering wordt symptomatische behandeling geadviseerd.
Belangrijke onverenigbaarheden:
Geen bekend.
7. Bijwerkingen
Honden.
| Zeer zelden (< 1 dier/10.000 behandelde dieren, inclusief geïsoleerde meldingen): | Braken1, Diarree.1 Overgevoeligheidsreactie (allergische huidreacties2), anafylaxie2 |
1) De behandeling kan worden gestaakt afhankelijk van de ernst van de bijwerkingen en een baten-risicobeoordeling door de dierenarts.
2) In deze gevallen moet de toediening worden gestopt en moet een symptomatische behandeling worden gegeven.
Het melden van bijwerkingen is belangrijk. Op deze manier kan de veiligheid van een diergeneesmiddel voortdurend worden bewaakt. Indien u bijwerkingen vaststelt, zelfs wanneer die niet in deze bijsluiter worden vermeld, of u vermoedt dat het geneesmiddel niet heeft gewerkt, neem dan in eerste instantie contact op met uw dierenarts. U kunt bijwerkingen ook melden aan de houder van de vergunning voor het in de handel brengen of de lokale vertegenwoordiger van de houder van de vergunning voor het in de handel brengen met behulp van de contactgegevens aan het einde van deze bijsluiter of via uw nationale meldsysteem:
8. Dosering voor elke diersoort, toedieningswijzenen toedieningswegen
Oraal gebruik
De aanbevolen dosering van het diergeneesmiddel is tweemaal daags 10 mg amoxicilline / 2,5 mg clavulaanzuur per kg lichaamsgewicht, d.w.z. 1 tablet per 60 kg lichaamsgewicht elke 12 uur, gedurende 5 tot 7 dagen, volgens de volgende tabel:
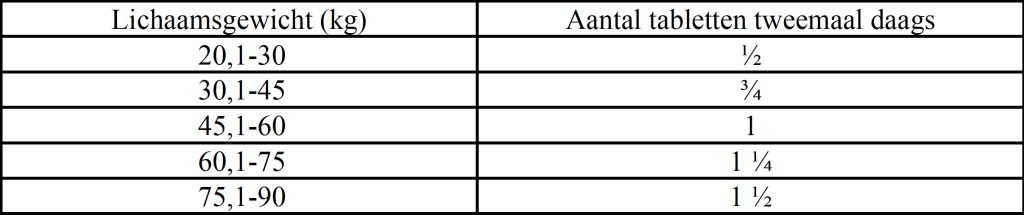
In ernstige gevallen kan de dosis verdubbeld worden overeenkomstig de beoordeling van de behandelende dierenarts.
Duur van de behandeling:
Voor alle indicaties is een behandeling van 5 tot 7 dagen in de meeste gevallen voldoende.
Voor chronische of recidiverende gevallen kan het nodig zijn om de behandeling 2 tot 4 weken voort te zetten.
9. Aanwijzingen voor een juiste toediening
Om een juiste dosering te waarborgen, dient het lichaamsgewicht zo nauwkeurig mogelijk bepaald te worden.
10. Wachttijd(en)
Niet van toepassing.
11. Bijzondere bewaarvoorschriften
Buiten het zicht en bereik van kinderen bewaren.
Dit diergeneesmiddel vereist geen bijzondere bewaarvoorschriften. Houdbaarheid na eerste opening van de primaire verpakking: 48 uur.
Doe elk deel van een tablet terug in de geopende blisterverpakking en gebruik deze binnen 48 uur.
Dit diergeneesmiddel niet gebruiken na de uiterste gebruiksdatum vermeld op de buitenverpakking na EXP.
De uiterste gebruiksdatum verwijst naar de laatste dag van de maand.
12. Speciale voorzorgsmaatregelen voor het verwijderen
Geneesmiddelen mogen niet verwijderd worden via afvalwater of huishoudelijk afval.
Maak gebruik van terugnameregelingen voor de verwijdering van ongebruikte diergeneesmiddelen of uit het gebruik van dergelijke middelen voortvloeiend afvalmateriaal in overeenstemming met de lokale voorschriften en nationale inzamelingssystemen die van toepassing zijn. Deze maatregelen dragen bij aan de bescherming van het milieu.
Vraag aan uw dierenarts of apotheker wat u met overtollige diergeneesmiddelen dient te doen.
13. Indeling van het diergeneesmiddel
Diergeneesmiddel op voorschrift.
14. Nummers van de vergunningen voor het in de handel brengen en verpakkingsgrootten
REG NL 127689
Verpakkingsgrootten van 10, 100, 250, 600 tabletten. Het kan voorkomen dat niet alle verpakkingsgrootten in de handel worden gebracht.
15. Datum waarop de bijsluiter voor het laatst is herzien
28 februari 2025
Gedetailleerde informatie over dit diergeneesmiddel is beschikbaar in de diergeneesmiddelendatabank van de Unie (https://medicines.health.europa.eu/veterinary).
16. Contactgegevens
Houder van de vergunning voor het in de handel brengen en fabrikant verantwoordelijk voor vrijgifte en contactgegevens voor het melden van vermoedelijke bijwerkingen:
Vetoquinol B.V.,
Postbus 9202,
4801 LE Breda,
Tel: +31 10 498 00 79
Fabrikant verantwoordelijk voor vrijgifte:
Vetoquinol
S.A Magny-Vernois
70200 Lure,
Frankrijk.
17. Overige informatie
Kanalisatie
UDD