
Kesium 500 mg/125 mg kauwtabletten
1. Naam van het diergeneesmiddel
Kesium 500 mg/125 mg kauwtabletten voor honden
2. Samenstelling
Per tablet:
Werkzame bestanddelen:
Amoxicilline (als amoxicillinetrihydraat) 500,00 mg
Clavulaanzuur (als kaliumclavulanaat) 125,00 mg
Klavervormig beige kauwtablet met breukstrepen. De tablet kan in vier gelijke delen verdeeld worden.
3. Doeldiersoort(en)
Hond.
4. Indicaties voor gebruik
Voor de behandeling van de volgende infecties veroorzaakt door β-lactamase producerende stammen van bacteriën die gevoelig zijn voor amoxicilline in combinatie met clavulaanzuur en waarbij uit klinische ervaring en/of gevoeligheidstesten blijkt dat dit diergeneesmiddel geschikt is:
- Huidinfecties (inclusief oppervlakkige en diepe pyodermieën) geassocieerd met Staphylococcus spp.
- Urineweginfecties geassocieerd met Staphylococcus spp., Streptococcus spp., Escherichia coli en Proteus mirabilis.
- Luchtweginfecties geassocieerd met Staphylococcus spp., Streptococcus spp. en Pasteurella spp.
- Maagdarminfecties geassocieerd met Escherichia coli.
- Infecties van de mondholte (mucosa) geassocieerd met Pasteurella spp., Streptococcus spp. en Escherichia coli.
5. Contra-indicaties
Niet gebruiken bij overgevoeligheid voor penicillines, voorandere stoffen van de β-lactam groep of één van de hulpstoffen.
Niet gebruiken bij dieren met een ernstig verstoorde nierfunctie die gepaard gaat met anurie en oligurie.
Niet toedienen aan gerbils, cavia’s, hamsters, konijnen en chinchilla’s. Niet gebruiken bij paarden en herkauwers.
Niet gebruiken in gevallen van bekende resistentie tegen deze combinatie.
6. Speciale waarschuwingen
Speciale voorzorgsmaatregelen voor veilig gebruik bij de doeldiersoort(en):
Wanneer het diergeneesmiddel wordt gebruikt dient rekening gehouden te worden met het officiële en nationale beleid ten aanzien van antimicrobiële middelen.
Niet gebruiken in die gevallen waarbij bacteriën gevoelig zijn voor smal spectrum penicillines of amoxicilline als enkelvoudig diergeneesmiddel.
Het wordt aanbevolen om voor aanvang van de behandeling een geschikte gevoeligheidstest uit te voeren en de behandeling alleen voort te zetten nadat gevoeligheid voor de combinatie is vastgesteld. Wanneer het diergeneesmiddel anders wordt gebruikt dan aangegeven in de SPC kan dit het aantal bacteriën dat resistent is tegen amoxicilline/clavulaanzuur verhogen en de effectiviteit van behandeling met β-lactam antibiotica verminderen vanwege de mogelijkheid van kruisresistentie.
Bij dieren met lever- en nierproblemen dient het doseringsschema zorgvuldig te worden geëvalueerd en dient het gebruik gebaseerd te zijn op een baten/risico beoordeling door de behandelend dierenarts.
Voorzichtigheid is geboden bij het gebruik bij andere kleine herbivoren dan die genoemd in sectie “Contra-indicaties”.
De mogelijkheid tot allergische kruisreacties met andere penicilline-derivaten en cephalosporines moet steeds in acht genomen worden.
De kauwtabletten zijn smakelijk.
Om eventuele accidentele inname te voorkomen, dienen de tabletten buiten het bereik van de dieren bewaard te worden.
Speciale voorzorgsmaatregelen te nemen door de persoon die het diergeneesmiddel aan de dieren toedient:
Penicillines en cephalosporinen kunnen overgevoeligheid (allergie) veroorzaken na injectie, inhalatie, inname via de mond of huidcontact. Overgevoeligheid voor penicillines kan leiden tot kruisreacties met cephalosporinen en omgekeerd. Allergische reacties op deze stoffen kunnen soms ernstig zijn.
Vermijd het contact met dit diergeneesmiddel bij bekende overgevoeligheid voor deze stoffen of indien u geadviseerd is deze middelen niet te hanteren.
Hanteer dit diergeneesmiddel met grote zorgvuldigheid om blootstelling te voorkomen. Neem alle aanbevolen voorzorgsmaatregelen in acht.
Indien u verschijnselen (zoals huiduitslag) vertoont na blootstelling, dient onmiddellijk een arts te worden geraadpleegd en deze waarschuwing worden getoond. Zwelling van het gezicht, lippen of ogen of ademhalingsproblemen zijn ernstigere symptomen en vereisen dringende medische verzorging.
Handen wassen na gebruik..
Dracht en lactatie:
Uit laboratoriumonderzoek bij ratten en muizen zijn geen gegevens naar voren gekomen die wijzen op teratogene, foetotoxische of maternotoxische effecten.
De veiligheid van dit diergeneesmiddel is niet bewezen tijdens dracht of lactatie.
Het diergeneesmiddel bij drachtige en lacterende dieren alleen gebruiken overeenkomstig de baten/risico beoordeling door de behandelend dierenarts.
Interactie met andere geneesmiddelen en andere vormen van interactie:
Chlooramphenicol, macroliden, sulfonamiden en tetracyclinen kunnen de antibacteriële werking van penicillines remmen, door hun snelle bacteriostatische werking.
Penicillines kunnen het effect van aminoglycosiden doen toenemen.
Overdosering:
In geval van overdosering kunnen diarree, allergische reacties of andere symptomen zoals rusteloosheid of krampen optreden. Indien nodig dient een symptomatische behandeling te worden ingezet.
7. Bijwerkingen
Hond:
| Zeer zelden (<1 dier/10.000 behandelde dieren, inclusief geïsoleerde meldingen): |
| Maagdarmstoornissen (bv. Diarree of braken)1 Allergische reacties (bv. Huidreacties, anafylaxie)2 |
1 De behandeling kan worden stopgezet, afhankelijk van de ernst van de bijwerkingen en de baten-risicobeoordeling van de behandelend dierenarts.
2 In deze gevallen dient de toediening te worden gestaakt en een symptomatische behandeling te worden gegeven.
Het melden van bijwerkingen is belangrijk. Op deze manier kan de veiligheid van een diergeneesmiddel voortdurend worden bewaakt. Indien u bijwerkingen vaststelt, zelfs wanneer die niet in deze bijsluiter worden vermeld, of u vermoedt dat het geneesmiddel niet heeft gewerkt, neem dan in eerste instantie contact op met uw dierenarts. U kunt bijwerkingen ook melden aan de houder van de vergunning voor het in de handel brengen met behulp van de contactgegevens aan het einde van deze bijsluiter of via uw nationale meldsysteem.
8. Dosering voor elke diersoort, toedieningswijzen en toedieningswegen
Oraal gebruik.
De aanbevolen dosis van het diergeneesmiddel is 10 mg amoxicilline /2,5 mg clavulaanzuur per kg lichaamsgewicht tweemaal daags via orale toediening bij honden, i.e. 1 tablet per 50 kg lichaamsgewicht elke 12 uur, volgens onderstaande tabel:
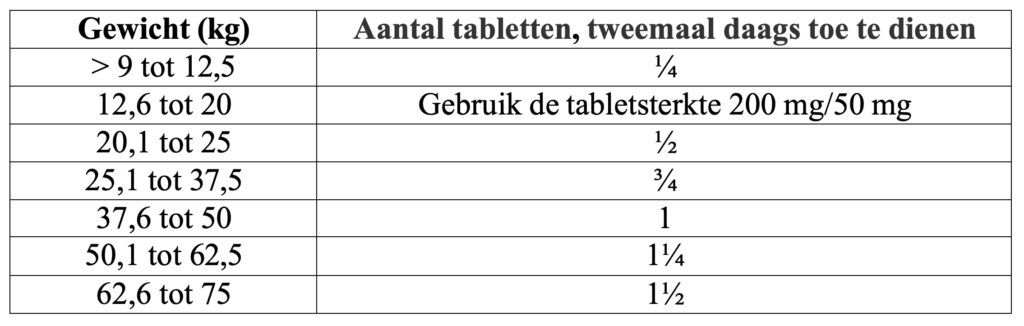
Bij hardnekkige infecties kan de dierenarts besluiten de dosering te verdubbelen tot 20 mg amoxicilline/5 mg clavulaanzuur per kg lichaamsgewicht 2 maal daags.
Behandelingsduur
De meerderheid van de routinegevallen reageert binnen 5 – 7 dagen behandeling.
In chronische gevallen kan een langere behandelingsduur noodzakelijk zijn. In deze omstandigheden dient de totale behandelingsduur door de dierenarts te worden vastgesteld, maar de behandelingsduur moet lang genoeg zijn om de bacteriële infectie volledig te genezen.
Om een juiste dosering te waarborgen dient het lichaamsgewicht zo nauwkeurig mogelijk bepaald te worden.
9. Aanwijzingen voor een juiste toediening
De kauwtabletten zijn smakelijk en worden door de meeste honden geaccepteerd. De kauwtabletten kunnen direct in de bek van het dier worden gegeven of met een kleine hoeveelheid voedsel.
Instructies voor het breken van de tablet: leg de tablet op een vlak oppervlak met de breuklijn naar beneden (de bolle kant naar boven). Oefen met de top van de wijsvinger een lichte verticale druk uit op het midden van de tablet om deze over de breedte in twee helften te breken. Om vervolgens een kwart te verkrijgen, oefen lichte druk uit met de wijsvinger op het midden van een helft om deze in twee delen te breken.
10. Wachttijd(en)
Niet van toepassing.
11. Bijzondere bewaarvoorschriften
Buiten het zicht en bereik van kinderen bewaren.
Niet bewaren boven 25 °C.
Halve tabletten moeten in de blister bewaard worden.
Resterende tabletdelen dienen na 36 uur weggegooid te worden.
Dit diergeneesmiddel niet gebruiken na de uiterste gebruiksdatum vermeld op de blister en buitenverpakking na Exp.
12. Speciale voorzorgsmaatregelen voor het verwijderen
Geneesmiddelen mogen niet verwijderd worden via afvalwater of huishoudelijk afval.
Maak gebruik van terugnameregelingen voor de verwijdering van ongebruikte diergeneesmiddelen of uit het gebruik van dergelijke middelen voortvloeiend afvalmateriaal in overeenstemming met de lokale voorschriften en nationale inzamelingssystemen die van toepassing zijn. Deze maatregelen dragen bij aan de bescherming van het milieu.
Vraag aan uw dierenarts of apotheker wat u met overtollige diergeneesmiddelen dient te doen.
13. Indeling van het diergeneesmiddel
Diergeneesmiddel op voorschrift.
14. Nummers van de vergunningen voor het in de handel brengen en verpakkingsgrootten
REG NL 112297
Verpakkingsgrootte:
Kartonnen doos met 6 tabletten.
Kartonnen doos met 12 tabletten.
Kartonnen doos met 96 tabletten.
Kartonnen doos met 144 tabletten.
Kartonnen doos met 240 tabletten.
Kartonnen doos met 480 tabletten.
Het kan voorkomen dat niet alle verpakkingsgrootten in de handel worden gebracht.
15. Datum waarop de bijsluiter voor het laatst is herzien
9 juni 2025
Gedetailleerde informatie over dit diergeneesmiddel is beschikbaar in de diergeneesmiddelendatabank van de Unie (https://medicines.health.europa.eu/veterinary).
16. Contactgegevens
Houder van de vergunning voor het in de handel brengen en contactgegevens voor het melden van vermoedelijke bijwerkingen:
Ceva Santé Animale NV/SA – Metrologielaan 6 – 1130 Brussel – België – Tel : 00 800 35 22 11 51
Fabrikant verantwoordelijk voor vrijgifte:
Ceva Santé Animale – Boulevard de la Communication – Zone Autoroutière – 53950 Louverné – Frankrijk
17. Overige informatie
KANALISATIE
UDD