
Synulox 250 mg tabletten
1. Naam van het diergeneesmiddel
Synulox 250 mg smakelijke tabletten voor honden en katten
2. Samenstelling
Per tablet:
Werkzamebestanddelen:
Amoxicilline 200 mg (overeenkomend met 229,57 mg amoxicilline trihydraat)
Clavulaanzuur 50 mg (overeenkomend met 59,56 mg kaliumclavulanaat)
Hulpstof:
Erythrosine (E127) 17,5 mg
Gespikkelde, roze, platte en ronde tabletten met afgeronde randen, een breukstreep aan de ene kant en de inscriptie SYNULOX aan de andere kant.
De tablet kan in twee gelijke delen worden verdeeld.
3. Doeldiersoort(en)
Hond en kat.
4. Indicaties voor gebruik
Honden:
Voor de behandeling van
- Huidinfecties (inclusief diepe en oppervlakkige pyodermie).
- Weke deleninfecties (inclusief anale sacculitis en abcessen).
- Urineweginfecties.
- Luchtweginfecties.
- Darminfecties.
- Parodontale infecties als aanvulling op mechanische of chirurgische parodontale behandeling.
Katten:
Voor de behandeling van
- Huidinfecties (inclusief oppervlakkige pyodermie).
- Weke deleninfecties (inclusief abcessen).
- Urineweginfecties.
- Luchtweginfecties.
- Darminfecties.
- Parodontale infecties als aanvulling op mechanische of chirurgische parodontale behandeling.
5. Contra-indicaties
Niet gebruiken bij konijnen, cavia’s, hamsters, gerbils, chinchilla’s of andere kleine herbivoren.
Niet gebruiken bij overgevoeligheid voor de werkzame bestanddelen, andere stoffen van de bètalactam groep of één van de hulpstoffen.
Niet toedienen aan paarden of herkauwende dieren.
Niet gebruiken bij dieren met ernstige nierfunctiestoornissen die gepaard gaan met anurie of oligurie.
6. Speciale waarschuwingen
Speciale waarschuwingen:
Kruisresistentie is aangetoond tussen amoxicilline/clavulaanzuur en andere antibiotica uit de bètalactam groep. Het gebruik van het diergeneesmiddel dient zorgvuldig te worden overwogen wanneer gevoeligheidstesten resistentie tegen andere antimicrobiële middelen uit de bètalactam groep hebben aangetoond, omdat de werkzaamheid verminderd kan zijn.
Wanneer gevoeligheidstesten resistentie tegen individuele bètalactamantibiotica hebben aangetoond, maar gevoeligheid voor de combinatie van amoxicilline/clavulaanzuur is bevestigd, kan behandeling met het diergeneesmiddel toch worden overwogen.
Niet gebruiken bij vermoedelijke of bevestigde infecties met meticillineresistente S. aureus (MRSA) en meticillineresistente S. pseudintermedius (MRSP), aangezien dergelijke isolaten als resistent moeten worden beschouwd tegen alle bètalactamantibiotica, inclusief amoxicilline/clavulaanzuurcombinaties.
Het diergeneesmiddel is niet werkzaam tegen infecties veroorzaakt door Pseudomonas spp. vanwege de inherente resistentie.
Speciale voorzorgsmaatregelen voor veilig gebruik bij de doeldiersoort(en):
Het gebruik van het diergeneesmiddel dient plaats te vinden op grond van identificatie en gevoeligheidstesten van de doelpathogeen/-pathogenen. Als dit niet mogelijk is, dient de behandeling gebaseerd te zijn op epidemiologische informatie en kennis van de gevoeligheid van de doelpathogenen op lokaal/regionaal niveau.
Het diergeneesmiddel dient gebruikt te worden in overeenstemming met het officiële, nationale en lokale beleid ten aanzien van antimicrobiële middelen.
Een antibioticum met een lager risico op selectie voor antimicrobiële resistentie (lagere AMEG-categorie) dient te worden gebruikt voor eerstelijnsbehandeling wanneer gevoeligheidstesten de waarschijnlijke werkzaamheid van deze aanpak suggereren.
Smalspectrum antibiotica met een lager risico op selectie voor antimicrobiële resistentie dienen te worden gebruikt voor eerstelijnsbehandeling wanneer gevoeligheidstesten de waarschijnlijke werkzaamheid van deze aanpak suggereren.
De farmacokinetiek van de werkzame bestanddelen in het doelweefsel kan ook worden overwogen.
Het routinematig gebruik van systemische antibiotica bij darminfecties wordt afgeraden.
Orale behandeling met antibiotica kan leiden tot verstoring van de maagdarmflora, vooral bij langdurige behandeling.
In geval van nier- of leverinsufficiëntie dient het gebruik van het diergeneesmiddel te worden onderworpen aan een baten-risicobeoordeling door de behandelend dierenarts.
Speciale voorzorgsmaatregelen te nemen door de persoon die het diergeneesmiddel aan de dieren toedient:
Penicillines en cefalosporines kunnen overgevoeligheid (allergie) veroorzaken na injectie, inhalatie, inslikken of na contact met de huid. Overgevoeligheid voor penicillines kan leiden tot kruisreacties met cefalosporines en omgekeerd. Allergische reacties veroorzaakt door deze stoffen kunnen in sommige gevallen ernstig zijn.
Personen met bekende overgevoeligheid moeten contact met het diergeneesmiddel vermijden. Draag handschoenen bij het hanteren van dit diergeneesmiddel om huidcontact te vermijden.
Als u na blootstelling aan het diergeneesmiddel symptomen zoals huiduitslag en aanhoudende oogirritatie ontwikkelt, raadpleeg dan onmiddellijk een arts en toon de bijsluiter of het etiket. Zwelling van het gezicht, de lippen of de ogen, of ademhalingsproblemen zijn ernstigere symptomen die dringend medische hulp vereisen.
Handen wassen na gebruik.
Om te voorkomen dat kinderen toegang krijgen tot het diergeneesmiddel, moet alleen het benodigde aantal tabletten uit de blisterverpakking worden gehaald en alleen wanneer nodig. Bewaar ongebruikte tabletten in de geopende blisterverpakking en doe deze direct na gebruik terug in de doos. De doos moet buiten het zicht en bereik van kinderen te worden bewaard. Raadpleeg bij accidentele inname onmiddellijk een arts en toon de bijsluiter of het etiket.
Dracht en lactatie:
De veiligheid van het diergeneesmiddel is niet bewezen tijdens dracht en lactatie.
In laboratoriumonderzoeken (rat, muis) konden alleen bij hoge doses tekenen van embryotoxiciteit of teratogeniteit worden vastgesteld.
Uitsluitend gebruiken overeenkomstig de baten-risicobeoordeling door de behandelende dierenarts.
Interactie met andere geneesmiddelen en andere vormen van interactie:
De bactericide werking van amoxicilline kan worden geremd door het gelijktijdig gebruik van bacteriostatische antimicrobiële middelen.
Penicillines kunnen de werking van aminoglycosiden versterken.
Overdosering:
Doseringen tot 40 mg amoxicilline en 10 mg clavulaanzuur/kg en 60 mg amoxicilline en 15 mg clavulaanzuur/kg, tweemaal daags toegediend gedurende 5 dagen, werden goed verdragen door respectievelijk jonge honden en jonge katten.
In de betreffende onderzoeken werden geen andere ongewenste effecten opgemerkt die met overdosering in verband gebracht werden, dan die genoemd in de rubriek ‘Bijwerkingen’ (voor informatie over symptomatische behandeling, zie ook de rubriek ‘Bijwerkingen’).
Vanwege de neurotoxiciteit van penicillines kan overdosering leiden tot symptomen van het centrale zenuwstelsel en convulsies. In deze gevallen moet de behandeling met het diergeneesmiddel onmiddellijk worden gestaakt en moet symptomatische behandeling worden gestart.
7. Bijwerkingen
Hond en kat:
| Vaak (1 tot 10 dieren/100 behandelde dieren): |
| maagdarmaandoeningen1 (bijv. braken, diarree) |
| Soms (1 tot 10 dieren/1.000 behandelde dieren): |
| hypersalivatie anorexie1,2, lethargie |
| Zeer zelden (<1 dier/10.000 behandelde dieren, inclusief geïsoleerde meldingen): |
| overgevoeligheidsreactie3 (bijv. allergische huidreactie, anafylaxie) |
1 Afhankelijk van de ernst van de bijwerking moet de behandeling worden gestaakt en moet symptomatische behandeling worden gestart, op basis van de baten-risicobeoordeling door de behandelende dierenarts.
2 Zeer zelden (<1 dier/10.000 behandelde dieren, inclusief geïsoleerde rapporten) bij katten.
3 Kan ernstig zijn. Onmiddellijke stopzetting van het diergeneesmiddel is vereist. Door de dierenarts te nemen tegenmaatregelen in geval van een allergische reactie:
- anafylaxie: dien epinefrine (adrenaline) en glucocorticoïden toe.
- allergische huidreacties: dien antihistaminica en/of glucocorticoïden toe.
Het melden van bijwerkingen is belangrijk. Op deze manier kan de veiligheid van een diergeneesmiddel voortdurend worden bewaakt. Indien u bijwerkingen vaststelt, zelfs wanneer die niet in deze bijsluiter worden vermeld, of u vermoedt dat het geneesmiddel niet heeft gewerkt, neem dan in eerste instantie contact op met uw dierenarts. U kunt bijwerkingen ook melden aan de houder van de vergunning voor het in de handel brengen met behulp van de contactgegevens aan het einde van deze bijsluiter of via uw nationale meldsysteem.
8. Dosering voor elke diersoort, toedieningswijzen en toedieningswegen
Oraal gebruik.
Dosering: 10 mg amoxicilline en 2,5 mg clavulaanzuur/kg lichaamsgewicht elke12 uur.
Bij hardnekkige luchtweginfecties kan de dosis worden verdubbeld tot 20 mg amoxicilline en 5 mg clavulaanzuur/kg lichaamsgewicht elke 12 uur en kan de behandeling tot 10 dagen worden verlengd.
Doseringsinstructies:
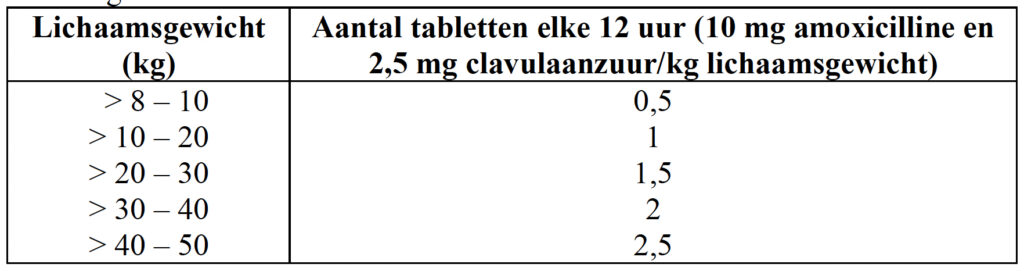
Behandelingsduur:
In de meeste gevallen is een behandelingsduur van 5 tot 7 dagen voldoende. Voor chronische gevallen kan een langere behandelingsduur nodig zijn.
Op basis van klinische proeven worden de volgende behandelingsduren aanbevolen: Chronische huidinfecties: 10-20 dagen.
Chronische blaasontsteking: 10-28 dagen.
9. Aanwijzingen voor een juiste toediening
Om een juiste dosering te waarborgen dient het lichaamsgewicht zo nauwkeurig mogelijk bepaald te worden.
De tabletten kunnen rechtstreeks in de bek van het dier worden toegediend of worden verkruimeld en aan een kleine hoeveelheid voer worden toegevoegd, dat direct gevoerd wordt.
10. Wachttijd(en)
Niet van toepassing.
11. Bijzondere bewaarvoorschriften
Buiten het zicht en bereik van kinderen bewaren.
Niet bewaren boven 25 °C.
Bewaren op een droge plaats.
Bewaar eventuele resterende halve tabletten in de blisterverpakking in de originele doos.
Dit diergeneesmiddel niet gebruiken na de uiterste gebruiksdatum vermeld op het etiket na Exp. De uiterste gebruiksdatum verwijst naar de laatste dag van die maand.
Houdbaarheid na delen van de tablet: 24 uur.
12. Speciale voorzorgsmaatregelen voor het verwijderen
Geneesmiddelen mogen niet verwijderd worden via afvalwater of huishoudelijk afval.
Maak gebruik van terugnameregelingen voor de verwijdering van ongebruikte diergeneesmiddelen of uit het gebruik van dergelijke middelen voortvloeiend afvalmateriaal in overeenstemming met de lokale voorschriften en nationale inzamelingssystemen die op het desbetreffende diergeneesmiddel van toepassing zijn.
Vraag aan uw dierenarts of apotheker wat u met overtollige diergeneesmiddelen dient te doen.
13. Indeling van het diergeneesmiddel
Diergeneesmiddel op voorschrift.
14. Nummers van de vergunningen voor het in de handel brengen en verpakkingsgrootten
REG NL 132207
Verpakkingsgrootten:
Kartonnen doos met 10 tabletten (1 blisterverpakking x 10 tabletten).
Kartonnen doos met 100 tabletten (10 blisterverpakkingen x 10 tabletten).
Kartonnen doos met 250 tabletten (25 blisterverpakkingen x 10 tabletten).
Het kan voorkomen dat niet alle verpakkingsgrootten in de handel worden gebracht.
15. Datum waarop de bijsluiter voor het laatst is herzien
17 november 2025
Gedetailleerde informatie over dit diergeneesmiddel is beschikbaar in de diergeneesmiddelendatabank van de Unie (https://medicines.health.europa.eu/veterinary).
16. Contactgegevens
Houder van de vergunning voor het in de handel brengen en contactgegevens voor het melden van vermoedelijke bijwerkingen:
Zoetis B.V.
Rivium Westlaan 74
NL-2909 LD Capelle aan den IJssel
Tel: +31 (0)10 714 0900
Fabrikant verantwoordelijk voor vrijgifte:
Haupt Pharma Latina S.r.l
Strada Statale 156 Dei Monti Lepini Km 47,600
Latina
Italië
Kanalisatie
UDD