
Zodon tabletten 88 mg
1. Naam en adres van de houder van de vergunning voor het in de handel brengen en de fabrikant verantwoordelijk voor vrijgifte, indien verschillend
Houder van de vergunning voor het in de handel brengen: Ceva Santé Animale B.V.
Tiendweg 8 c
2671 SB Naaldwijk Nederland
Fabrikant verantwoordelijk voor vrijgifte:
CEVA SANTE ANIMALE CEVA SANTE ANIMALE
BOULEVARD DE LA COMMUCATION
200 Avenue de Mayenne Zone Autoroutière Zone industrielle des Touches 53950 LOUVERNE 53000 LAVAL Frankrijk
Frankrijk Tel: 33 2 43 49 51 51
Tel: 33 2 43 49 51 51 Fax: 33 2 43 53 97 00
Fax: 33 2 43 53 97 00 E-mail: sogeval@sogeval.fr E-mail: sogeval@sogeval.fr
2. Benaming van het diergeneesmiddel
Zodon vet 88 mg kauwtabletten voor honden Clindamycine (als hydrochloride)
3. Gehalte aan werkza(a)m(e) en overige bestandd(e)el(en)
Per tablet:
Werkzaam bestanddeel:
Clindamycine (als hydrochloride)…………………………………….88 mg
Kauwtablet
Klavervormige beige tablet met breukstrepen. De tablet kan in vier gelijke delen gedeeld worden.
4. Indicaties
– Voor de behandeling van geïnfecteerde wonden, abcessen en mondholte / tandheelkundige infecties veroorzaakt door of geassocieerd met Staphylococcus spp, Streptococcus spp (met uitzondering van Streptococcus faecalis), Bacteroides spp, Fusobacterium necrophorum en Clostridium perfringens
– Voor de behandeling van oppervlakkige pyodermie, geassocieerd met Staphylococcus pseudintermedius
– Voor de behandeling van osteomyelitis veroorzaakt door Staphylococcus aureus
5. Contra-indicaties
Niet gebruiken bij overgevoeligheid voor het werkzame bestanddeel of voor (één van) de hulpstoffen of voor lincomycine.
Niet toedienen aan konijnen, hamsters, cavia’s, chinchilla’s, paarden of herkauwers omdat de inname van clindamycine bij deze diersoorten kan leiden tot ernstige spijsverteringsstoornissen.
6. Bijwerkingen
Braken en diarree werd soms waargenomen.
Clindamycine veroorzaakt soms een overgroei van niet-gevoelige organismen zoals clostridia en gisten. In geval van superinfectie dienen geschikte maatregelen te worden genomen, overeenkomstig de klinische toestand
Indien u ernstige bijwerkingen of andersoortige reacties vaststelt die niet in deze bijsluiter worden vermeld, wordt u verzocht uw dierenarts hiervan in kennis te stellen.
7. Diersoort waarvoor het diergeneesmiddel bestemd is
Hond.
8. Dosering voor elke doeldiersoort, wijze van gebruik en toedieningsweg
Voor orale toediening.
1. Dien voor de behandeling van geïnfecteerde wonden en abcessen en mondholte/ tandheelkundige infecties één van de volgende doseringen toe:
– 5,5 mg/kg lichaamsgewicht om de 12 uur gedurende 7-10 dagen, of
– 11 mg/kg lichaamsgewicht om de 24 uur gedurende 7-10 dagen
Indien er binnen de 4 dagen geen klinisch effect wordt waargenomen, heroverweeg de diagnose dan
2. Dien voor de behandeling van oppervlakkige pyodermie bij honden, één van de volgende doseringen toe:
– 5,5 mg/kg lichaamsgewicht om de 12 uur, of
– 11 mg/kg lichaamsgewicht om de 24 uur
Voor de behandeling van oppervlakkige pyodermie wordt meestal een behandelingsduur van 21 dagen aanbevolen met een verlenging van de behandeling gebaseerd op een klinische beoordeling.
3. Dien voor de behandeling van osteomyelitis bij honden, het volgende toe:
– 11 mg/kg lichaamsgewicht om de 12 uur gedurende minimaal 28 dagen
Indien er binnen de 14 dagen geen klinisch effect wordt waargenomen, dan dient de behandeling gestaakt en de diagnose herzien te worden.
Bijvoorbeeld:
• Voor een doseringsschema van 11 mg/kg
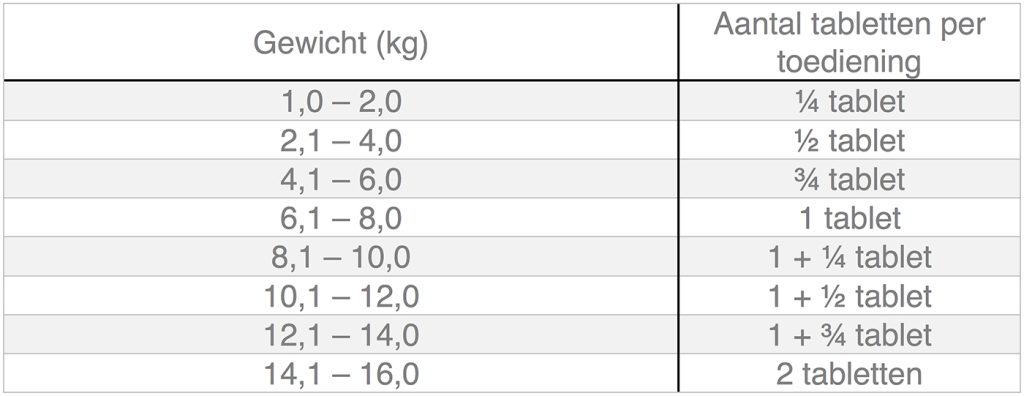
• Voor een doseringsschema van 5,5 mg/kg
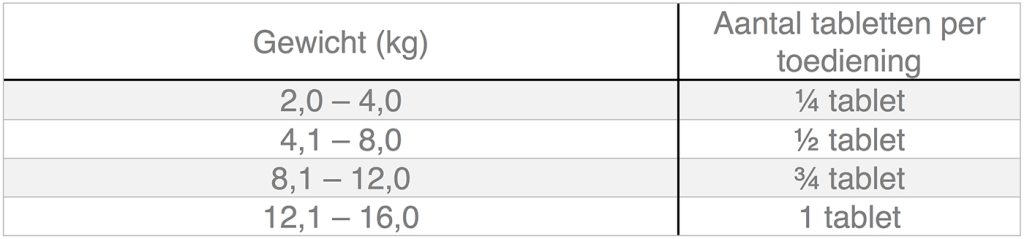
Teneinde een juiste dosering te berekenen, dient het lichaamsgewicht zo nauwkeurig mogelijk te worden bepaald. Dit om onderdosering te vermijden.
9. Aanwijzingen voor een juiste toediening
De tabletten bevatten een smaakstof. Ze kunnen direct worden toegediend in de mond van de dieren of toegevoegd worden aan een kleine hoeveelheid voedsel.
10. Wachttermijn
Niet van toepassing.
11. Speciale voorzorgsmaatregelen bij bewaren
Buiten het zicht en bereik van kinderen bewaren. Bewaren beneden 30 °C.
Tabletgedeeltes dienen in de blisterverpakking bewaard te worden.
Overgebleven tabletgedeeltes dienen na 72 uur afgevoerd te worden. Bewaar de blister in de buitenverpakking.
Niet gebruiken na de uiterste gebruiksdatum vermeld op de doos en de blister na EXP. De uiterste gebruiksdatum verwijst naar de laatste dag van de maand.
12. Speciale waarschuwingen
Speciale waarschuwingen voor elke diersoort waarvoor het diergeneesmiddel bestemd is: Geen.
Speciale voorzorgsmaatregelen voor gebruik bij dieren:
De kauwtabletten bevatten een smaakstof. Bewaar de tabletten buiten het bereik van de dieren, om accidentele inname te voorkomen.
Het gebruik van het diergeneesmiddel dient plaats te vinden op grond van gevoeligheidstesten van uit het dier geïsoleerde bacteriën.
Wanneer het diergeneesmiddel wordt gebruikt dient rekening gehouden te worden met het officiële en nationale beleid ten aanzien van antimicrobiële middelen. Wanneer het diergeneesmiddel anders wordt gebruikt dan aangegeven in de SPC kan dit het aantal bacteriën dat resistent is tegen clindamycine verhogen en de effectiviteit van behandeling met lincomycine of macrolide antibiotica verminderen vanwege de mogelijkheid van kruisresistentie.
Clindamycine vertoont een parallelle resistentie met erythromycine. Er werd een gedeeltelijke kruisresistentie aangetoond tussen clindamycine, erythromycine en andere macrolide antibiotica. Tijdens een langdurige behandeling van een maand of langer, moeten testen met betrekking tot lever- en nierfunctie en het bloedbeeld regelmatig worden uitgevoerd.
Bij dieren met ernstige nierproblemen en/of zeer ernstige leverproblemen, gepaard gaande met ernstige metabole afwijkingen, moet de toe te dienen dosis zorgvuldig worden vastgesteld en hun
toestand moet bij behandeling met een hoge dosis van clindamycine worden gecontroleerd door het uitvoeren van bloedonderzoeken.
Het gebruik van het diergeneesmiddel wordt niet aanbevolen bij zogende pups.
Speciale voorzorgsmaatregelen, te nemen door degene die het diergeneesmiddel aan de dieren toedient:
Personen met een bekende overgevoeligheid voor lincosamiden ( lincomycine en clindamycine ) moeten contact met het diergeneesmiddel vermijden.
Was de handen na aanraking van de tabletten.
Accidentele inname kan leiden tot spijsverteringsproblemen, zoals abdominale pijn en diarree. Voorzichtigheid moet betracht worden om accidentele inname te voorkomen.
In geval van accidentele inname, vooral door kinderen, dient onmiddellijk een arts te worden geraadpleegd en de bijsluiter of het etiket te worden getoond.
Gebruik tijdens dracht en lactatie:
Hoewel studies met hoge doseringen bij ratten suggereren dat clindamycine niet teratogeen is en de fokprestaties van mannelijke- en vrouwelijke dieren niet significant beïnvloedt, werd de veiligheid van het diergeneesmiddel bij drachtige teven of mannelijke fokreuen niet vastgesteld.
Clindamycine passeert de placenta en de bloed-melk barrière.
De behandeling van lacterende teven kan diarree veroorzaken bij de pups.
Uitsluitend gebruiken overeenkomstig de baten/risicobeoordeling door de behandelend dierenarts.
Interacties met andere geneesmiddelen en andere vormen van interactie:
Van clindamycine hydrochloride werd aangetoond dat het neuromusculair blokkerende eigenschappen heeft die de werking van andere neuromusculair blokkerende stoffen kunnen versterken. Dit diergeneesmiddel dient met voorzichtigheid te worden gebruikt bij dieren die dergelijke stoffen toegediend krijgen.
Clindamycine dient niet gecombineerd te worden met erythromycine of andere macroliden teneinde de macrolide-geïnduceerde resistentie tegen clindamycine te voorkomen.
Clindamycine kan de plasmaspiegels van cyclosporine verminderen met het risico op gebrek aan werkzaamheid.
Bij gelijktijdig gebruik van clindamycine en aminoglycosiden (bijv. gentamicine), kan een risico op nadelige interacties (acuut nierfalen) niet worden uitgesloten.
Overdosering (symptomen, procedures in noodgevallen, antidota):
Bij honden leidden orale doseringen van clindamycine tot 300 mg/kg/dag niet tot toxiciteit. Honden die 600 mg/kg/dag clindamycine toegediend kregen, ontwikkelden anorexia, braken en gewichtsverlies. In geval van een overdosis, de behandeling onmiddellijk stopzetten en een symptomatische behandeling starten.
13. Speciale voorzorgsmaatregelen voor het verwijderen van niet-gebruikte diergeneesmiddelen of eventuele restanten hiervan
Ongebruikte diergeneesmiddelen of restanten hiervan dienen in overeenstemming met de nationale vereisten te worden verwijderd.
14. De datum waarop de bijsluiter voor het laatst is herzien
13 september 2016
15. Overige informatie
Verpakkingsgrootten:
Kartonnen doos met 10 tabletten. Kartonnen doos met 20 tabletten. Kartonnen doos met 100 tabletten. Kartonnen doos met 120 tabletten. Kartonnen doos met 240 tabletten.
Het kan voorkomen dat niet alle verpakkingsgrootten in de handel worden gebracht.
Voor meer informatie over het diergeneesmiddel kunt u contact opnemen met de lokale vertegenwoordiger van de houder van de vergunning voor het in de handel brengen.
REG NL 113790
KANALISATIE
UDD